◆ 新薬情報 index
2025年6月製造販売承認
(印刷用画面へ)■ベルスピティ錠2mg ■デュピクセント皮下注300mg ペン、皮…
■ デュピクセント皮下注300mg ペン、皮下注300mg シリンジ、皮下注200mg シリンジ
|
| 1. 承認概要 | ||
| 新有効成分 2025年6月 / 2018年4月 発売 | ||
| 2. 薬効分類名 | ||
| ヒト型抗ヒトIL-4/13受容体モノクローナル抗体 | ||
| 3. 一般的名称 | ||
| デュピルマブ(遺伝子組換え) | ||
| 4. 適応症 | ||
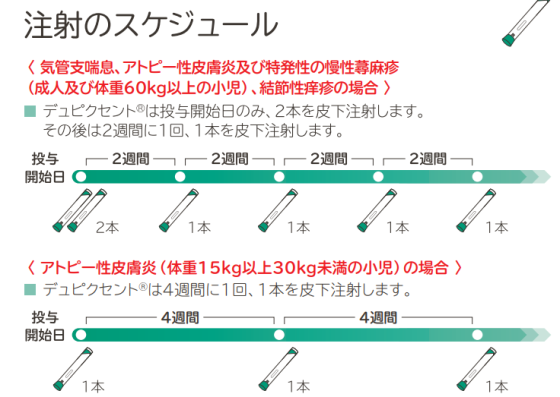
| ■300mgペン、300mgシリンジ 既存治療で効果不十分な下記皮膚疾患 ○アトピー性皮膚炎 ○結節性痒疹 ○特発性の慢性蕁麻疹 ○ 気管支喘息(既存治療によっても喘息症状をコントロールできない重症又は難治の患者に限る) ○慢性閉塞性肺疾患(既存治療で効果不十分な患者に限る) ○ 鼻茸を伴う慢性副鼻腔炎(既存治療で効果不十分な患者に 限る) ■200mgシリンジ 既存治療で効果不十分な下記皮膚疾患 ○アトピー性皮膚炎 ○特発性の慢性蕁麻疹 ■添付文書 ■患者向け医薬品ガイド ■RMP患者向け資材:デュピクセント 自己注射のためのガイドブック | ||
| 5. 類薬との比較 | ||
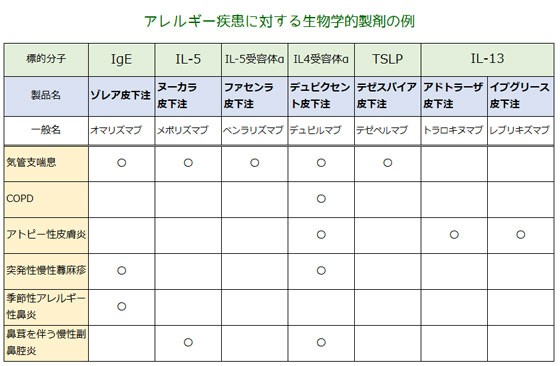 ■ アドトラーザ皮下注150mgシリンジ/皮下注300gmペン https://www.shimo-web.com/DI2023/sinyaku.php?ID=nd-2212adtralza ■ミチーガ皮下注用60mgシリンジ https://www.shimo-web.com/DI2023/sinyaku.php?ID=nd-2203mitchga ■エキシデンサー皮下注は26週間(6ヶ月)に1回という長時間作用型の生物学的製剤で2025年12月に承認されました。 | ||
| 6. 特徴 | ||
| 【特徴】 本剤は、「重症アトピー性皮膚炎の治療を大きく変えた」と言われるほどの画期的な薬剤です。 アトピー性皮膚炎や気管支喘息の治療薬として、2018年に日本で初めての抗体医薬として承認されましたが、その後、適応が拡大され、2023年6月には結節性痒疹、2024年2月には特発性の慢性蕁麻疹、さらに、2025年4月にはCOPDに対する適応が追加されました。 【承認状況】 〈アトピー性皮膚炎〉 我が国では、2018 年1 月に「既存治療で効果不十分なアトピー性皮膚炎」の適応で製造販売承認を取得し、2023 年9 月、生後6 カ月以上の小児に対する用法及び用量の追加承認、およびデュピクセント皮下注200mg シリンジの製造販売承認を取得しました。 〈気管支喘息〉 2019 年3 月には「気管支喘息(既存治療によっても喘息症状をコントロールできない重症又は難治の患者に限る)」の追加効能が承認されました。 〈鼻茸を伴う慢性副鼻腔炎〉 2020 年3 月には「鼻茸を伴う慢性副鼻腔炎(既存治療で効果不十分な患者に限る)」の追加効能が承認されました。 〈結節性痒疹〉 2023 年6 月に「既存治療で効果不十分な結節性痒疹」の追加効能が承認されました。 〈特発性の慢性蕁麻疹〉 2024 年2 月に「既存治療で効果不十分な特発性の慢性蕁麻疹」の追加効能が承認されました。 〈特発性の慢性蕁麻疹〉 2024 年2 月に「既存治療で効果不十分な特発性の慢性蕁麻疹」の追加効能が承認されました。 〈慢性閉塞性肺疾患〉 2025 年3 月に「慢性閉塞性肺疾患(既存治療で効果不十分な患者に限る)」の追加効能が承認されました。 【作用機序】 この薬は、ヒト型抗ヒトインターロイキン(IL)-4/13 受容体モノクローナル 抗体製剤と呼ばれる注射薬です。「IL-4」と「IL-13」というサイトカインの働きを直接抑えることで、アトピー性皮膚炎の病態や喘息の気道炎症、鼻茸を伴う慢性副鼻腔炎、慢性閉塞性肺疾患に関与する Type 2 炎症反応を抑制し、症状を改善します 【用法・用量】 〈アトピー性皮膚炎〉 成人には初回に600mgを皮下投与し、その後は 1 回300mgを 2 週間隔で皮下投与します。 〈結節性痒疹〉 成人には初回に600mgを皮下投与し、その後は 1 回300mgを 2 週間隔で皮下投与します。 〈特発性の慢性蕁麻疹〉 成人には初回に600mgを皮下投与し、その後は 1 回300mgを 2 週間隔で皮下投与します。 〈気管支喘息〉 成人及び12歳以上の小児には初回に600mgを皮下投与し、その後は 1 回300mgを 2 週間隔で皮下投与します。 〈慢性閉塞性肺疾患〉 成人には1 回300mgを 2 週間隔で皮下投与します。 〈鼻茸を伴う慢性副鼻腔炎〉 成人には1 回300mgを 2 週間隔で皮下投与します。なお、症状安定後には、1 回300mgを 4 週間隔で皮下投与できます。 【副作用】 重大な副作用として、重篤な過敏症が報告されています。また、主な副作用は、注射部位紅斑、結膜炎、口腔ヘルペス、アレルギー性結膜炎、好酸球増加症、注射部位反応、注射部位浮腫、頭痛、発疹、発熱、関節痛などが報告されています。 適応疾患で副作用報告は異なりますが、成人アトピー性皮膚炎患者を対象とした国際共同試験 3 試験で本剤 300 mg を 2 週に 1 回投与された 403 例(日本人 62 例を含む)において、副作用は 123 例に発現し、主な副作用は注射部位反応 29 例、頭痛 12 例、アレルギー性結膜炎 7 例でした(承認前)。
| ||
| 7. 使用上の注意と服薬支援 | ||
| 【薬剤師への注意】 アトピー性皮膚炎に使用する場合には、以下の方が対象となります。 1.通常の外用治療(ストロングクラス以上のステロイドやタクロリムス外用剤など)を6ヶ月以上行っても効果が期待できない方。 2.本剤投与時にアトピー性皮膚炎の病変部の状態に応じた抗炎症外用薬や保湿外用薬の外用剤を継続使用できる方。 【患者さんへの指導例】 1.皮下注射してください。 2.使用前に300mgシリンジおよび300mgペンは45分以上、200mg シリンジは30分以上かけて室温に戻してください。 3.使用直前までこの薬のキャップを外さず、キャップを外したら直ぐに使用して ください。 4.腹部、大腿部または上腕部に皮下注射してください。腹部へ皮下注射する場合 は、へその周り5cm は避けて注射してください。また、同じ箇所へ繰り返し注 射することは避けてください。 5.本剤投与中の生ワクチンの接種は、安全性が確認されていないので避けてください。 6.本剤が疾病を完治させる薬剤でなく、本剤投与中も保湿外用剤等を併用する必要があります。 7.冷蔵庫から取り出した後は、外箱に入れたまま25℃以下で保存し、14日以内に使用してください。 【ここがポイント!】 ・デュピクセントによる治療が受けられる人は、本剤の薬価が比較的高いので、問題なく費用負担ができる人が対象とならざるをえません。 ・自己注射も可能ですが、困難な場合は、2週間に1度程度の通院が可能な人が対象となります。 ・デュピクセント 300mg にはペンとシリンジの2種類の剤形があり、選択できます。ペンは注入ボタンがなく、皮膚に押しあてることで注射が可能です。
| ||
| 8. 製造販売元など | ||
| 製造販売元: サノフィ株式会社 (https://www.sanofi.co.jp/ja/contact) お問合せ先:くすり相談室 0120-109-905 月~金 9:00~17:00(祝日・会社休日を除く) <更新履歴> 2025.6 類薬比較表の更新、承認情報を改訂 2026.1 類薬比較表に用法の項目、小児適応の項目を追加、エキシデンサー皮下注を追加。 |
(文責 下平秀夫) 2025年6月/2026年1月更新